Zusammenfassung Neben den gesellschaftlich akzeptierten Substanzen wie Nikotin und Alkohol werden illegale Drogen entweder als Monosubstanzen, vielfach aber auch in Kombination konsumiert. Dabei muss der gelegentliche Konsum von regelmäßigem Gebrauch (im Rahmen einer Suchterkrankung) unterschieden werden. Ein Missbrauch von illegalen Drogen bei der Arbeit führt in der Regel zu arbeitsrechtlichen Konsequenzen, da durch den Konsum die Fähigkeit, die Arbeit verrichten zu können, ohne andere oder sich selbst zu gefährden, in aller Regel beeinträchtigt ist. An dieser Stelle nimmt der Betriebsarzt eine Schlüsselrolle ein. Einerseits ist er der Arbeitssicherheit verpflichtet, andererseits aber auch den Interessen des betroffenen Arbeitnehmers. Diese Übersicht soll den Arbeitsmediziner/Betriebsarzt mit der Vielfalt der auf dem illegalen Markt erhältlichen psychotropen Substanzen vertraut machen. Im Teil 3 werden im Rahmen der Substanzübersicht die Naturstoffe Salvinorin A und Cannabis sowie Wirkstoffe mit Angriffspunkt am N-Methyl-D-Aspartat (NMDA)-Rezeptor besprochen. Auf die deutlichen Unterschiede in der Risikobewertung für die Arbeitswelt zwischen den einzelnen Substanzen wird eingegangen (Wirkdauer, Nachweismöglichkeiten, Abhängigkeitsrisiko). Abschließend wird ein Konzept vorgestellt, das dem Arbeitsmediziner den Umgang mit der Problematik in der täglichen Praxis erleichtern soll. Schlüsselwörter
· Biodrogen
· Salvinorin A
· NMDA-Rezeptor- Antagonisten
· Drogenscreening am Arbeitsplatz
· Biodrugs
· Salvinorin A
· NMDA-receptor-antagonist
· Sscreening for illicit drugs at the workplace
3.4.3 Salvinorin A (Abbildung 14a)
Salvinorin A ist der einzige psychoaktive Vertreter der Stoffgruppe der Salvinorine. Das Diterpenoid kommt als Hauptwirkstoff natürlich im Aztekensalbei (Salvia divinorum, Abbildung 14b) in Mengen von maximal 3,7 mg/g Trockengewicht vor. Salvinorin A wurde als möglicher selektiver Agonist des k-Opioid-Rezeptors identifiziert. Der k-Agonismus könnte der Grund für die halluzinogene Wirkung sein; diese tritt schon bei Dosen zwischen 150 und 500 ?g auf. Salvinorin A unterscheidet sich in seiner Pharmakodynamik deutlich von den klassischen Halluzinogenen wie LSD. Im Gegensatz zu diesen wirkt Salvinorin A nicht am 5-HT2A-Rezeptor. Es sind etliche Verbindungen mit k-Opioid-agonistischer Wirkung bekannt, die eine halluzinogene Wirkung zeigen, darunter Pentazocin.42 Die Resorption nach oraler Aufnahme ist mäßig (intensives und langes Kauen der frischen Blätter erforderlich, durch Zusatz von Dimethylsulfoxid = DMSO erhebliche Verbesserung der Resorption); beim Rauchen besser.43 Der genaue Eliminationsweg ist noch nicht bekannt. Eine Einzeldosis von 0,11 mg (zwei bis acht zerkleinerte Blätter) führt nach wenigen Sekunden (Rauchen) bzw. 30 Minuten (orale Aufnahme) zum Wirkungsbeginn. Die Wirkdauer beträgt 30 Minuten (Rauchen) bzw. ein bis zwei Stunden nach oraler Aufnahme.10 Die psychoaktive Wirkung ist dosisabhängig bizarr und ungewöhnlich, sodass sie sich mit den bekannten Wirkungen von anderen bekannten euphorisierenden und psychedelischen Substanzen nicht vergleichen lässt. In niedriger Dosis kommt es zu halluzinogenen Rauschzuständen mit Farb- und Formverzerrung. Bei höheren Dosen (> 200 µg) wird eine unbeschreiblich bizarre Verzerrung der Bewusstseins- und Erlebniszustände beschrieben, identitätsauflösender als Ketamin und wirklichkeitsverzerrender als DMT: Erlebnis von Realität und Zeit als klebrige fassbare Objekte, die veränderbar sind.30 In den letzten Jahren ist ein Salvia-Boom zu beobachten, zumal die die Pflanze leicht zu kultivieren ist.
Der Eliminationsweg ist unbekannt und somit der Nachweis von Metaboliten bisher nicht möglich. Heute ist Salvia divinorum die meist gebrauchte Naturdroge in Deutschland.43
3.4.4 Psychedelische Wirkstoffe mit Angriffspunkt am N-Methyl-D-Aspartat (NMDA)-Rezeptor
Ketamin (Szenenamen: K, Kate, Barbara, Ket, Kitty, Kiti, Special K, Vitamin K, Multiketamin, Fiction, Keta) ist ein Cyclohexanderivat und wird als Arzneimittel in der Medizin zur Einleitung und Aufrechterhaltung einer Narkose, in der Schmerztherapie als Analgetikum und gegebenenfalls zur Behandlung von Asthma (Notfallnarkose bei therapierefraktärem Status asthmaticus) eingesetzt (Abbildung 15a). Ketamin nimmt durch die Auslösung einer dissoziativen Anästhesie eine Ausnahmestellung gegenüber Anästhetika ein (Bewusstseinsausschaltung und Schmerzfreiheit unter weitgehender Erhaltung der Schutzreflexe). Als Dissoziativum wird Ketamin auch illegal als Droge verwendet. Ein zunehmender Konsum wurde in den USA ab 1997 beobachtet. Die Substanz wurde auch im Rahmen von sogenannten near death parties konsumiert.
Im Rahmen eines Forschungsauftrages der Firma Parke-Davis bei der Suche nach einem Ersatz für das mit starken Nebenwirkungen behaftete Anästhetikum Phencyclidin (PCP) synthetisierte C. L. Stevens, Pharmakologe an der Wayne State University Detroit, 1962 erstmalig die Substanz Ketamin (Abbildung 15b und 15c). Im Jahre 1966 erhielt dann Parke-Davis ein Patent für die Herstellung von Ketamin als Arzneimittel sowohl für die Humanmedizin als auch für die Tiermedizin. Der klinische Pharmakologe E.F. Domino führte im August 1964 seinen ersten (nichtmedizinischen) Selbstversuch mit Ketamin durch und erkannte dabei das psychedelische Potenzial der Substanz. Die Bezeichnung dissoziatives Anästhetikum für Ketamin wurde von ihm dann im folgenden Jahr 1965 eingeführt. Im Vietnamkrieg erlangte Special K bei US-Soldaten als Schmerzmittel (und Droge) eine bedeutende Rolle.44
Wirkorte und -mechanismen der vielfältigen Ketamin-Effekte sind nicht restlos geklärt. Der Hauptwirkort befindet sich am Glutamat-NMDA-Rezeptorkomplex. Die Aminosäure Glutaminsäure ist ein wichtiger Neurotransmitter des Zentralnervensystems (siehe Teil 1 dieser Übersicht), wo sie einen Einstrom von Kalzium-Ionen bewirkt, der vielfältige intrazelluläre Prozesse induziert.39 Ketamin hat dort eine antagonistische Wirkung unter Vermittlung der Phencyclidin (PCP)-Bindungsstelle am NMDA-Rezeptor. Ketamin beeinflusst das cholinergene System, indem es die NMDA-Rezeptor-abhängige Acetylcholin-Freisetzung verhindert. Es hemmt ebenfalls andere Glutamatrezeptoren und zeigt darüber hinaus eine schwache agonistische Wirkung an Opioidrezeptoren sowie Affinität zu GABA-Rezeptoren (Allrounders). Weiterhin wirkt es hemmend auf die periphere Wiederaufnahme von Katecholaminen wie Noradrenalin und Dopamin an der synaptischen Endplatte mit Verstärkung endogener und exogener Katecholamineffekte. Durch diese Mechanismen kommt es zu einer ausgeprägten Stimulation des Herz-Kreislauf-Systems. Durch Überstimulation des Zentralnervensystems oder Induktion eines kataleptischen Zustandes wird eine Amnesie ausgelöst. Das thalamoneocorticale System wird gedämpft, das limbische aktiviert. Ketamin kann auf das periphere Nervensystem sowohl depressiv als auch exzitatorisch wirken. Es hat nur geringe viscerale analgetische Effekte, dafür aber ausgeprägte somatische. Weiterhin scheint Ketamin eine antidepressive Wirkkomponente zu besitzen, die bereits nach zwei Stunden einsetzt.45,46
Ketamin wird als Injektionsanästhetikum vertrieben. Die Lösungen werden für den Missbrauch eingetrocknet und das resultierende Pulver nasal appliziert (gesnieft). Auch die orale Aufnahme führt zu einer (abgeschwächten) Wirkung. Nach höherer Dosierung kommt es zu einer ca. zehn Minuten dauernden Bewusstlosigkeit und anschließend zu einem Dämmerschlaf von ein bis zwei Stunden Dauer. Stunden nach Abklingen des Rausches sind allgemeine Schwäche, motorische Koordinationsstörungen und Übelkeit möglich. Der Rausch selbst wird sehr unterschiedlich beschrieben. Seelenreisen, Nah-Tod-Erlebnisse (Gefühl von Frieden, Losgelöstheit vom Körper, Eintauchen in eine Welt der Dunkelheit, Gehen durch einen Tunnel, Wahrnehmen eines Lichtes, Eintreten in das Licht), Halluzinationen mit starken Farb-und Formveränderungen treten auf. Bei Mehrfachgebrauch ist eine Toleranzentwicklung zu beobachten, von physischer Abhängigkeit wurde bisher nicht berichtet. Bei chronischem Gebrauch besteht die Möglichkeit von hirnorganischen Schäden. Aufgrund seiner dissoziativen, bewusstseinsverändernden Wirkung ist Ketamin in vielen europäischen Ländern auch als Partydroge bekannt. Ketamin wird aber nicht nur als Partydroge gebraucht, sondern auch in der umstrittenen psycholytischen Psychotherapie angewendet.
Die Elimination erfolgt hepatisch und die Metaboliten werden renal ausgeschieden (HWZ 18 Stunden!). Diese sind im Urin bis zwei Tage nach einmaliger Gabe nachweisbar (Ketamin führt zu falsch positiven Drogenscreening-Tests auf PCP).
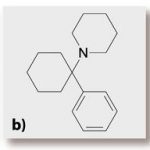
Phencyclidin (Abkürzung von Phenylcyclohexylpiperidin, kurz PCP; in der Drogenszene auch als Angel Dust, Engelsstaub, Londrea, Killerweed, Sherman Hemsley, TAC oder Peace Pill bekannt) ist ein missbräuchlich als Partydroge genutztes Dissoziativum (Abbildung 15b und c). Die Stammsubstanz Phencyclidin wurde 1926 erstmals synthetisiert. Nachdem ihre ruhigstellende Wirkung an Affen erfolgreich erprobt war, wurde Phencyclidin 1956 in Deutschland unter dem Handelsnamen Sernylan® als Tieranästhetikum auf den Markt gebracht. 1963 erfolgte die Zulassung als dissoziatives Anästhetikum unter dem Markennamen Sernyl®. Es wurde jedoch wegen seiner starken psychischen Nebenwirkungen bereits zwei Jahre später wieder vom Markt genommen. 1967 tauchte es erstmals bei einem Rockfestival in San Francisco in der Drogenszene auf und geriet wegen seiner falsch deklarierten Wirkung zunächst wieder in Vergessenheit. Aufgrund des Missbrauchpotenzials wurde der Einsatz als Tieranästhetikum gleichzeitig verboten. 1977 tauchte die Substanz bei in Deutschland stationierten US-Streitkräften wieder auf und erfuhr von dort eine Verbreitung in Untergrundlaboratorien, die Abwandlungen am Molekülgerüst vornahmen, um die halluzinogene Wirkung zu verstärken. Derzeit sind mehr als 125 Phencyclidin-Derivate bekannt.30
Insbesondere nach Langzeitgebrauch besteht die Gefahr einer psychischen Abhängigkeit.44 Phencyclidin wirkt durch Bindung am NMDA/PCP-Glutamat-Rezeptor-Kanal-Komplex als nichtkompetitiver Antagonist am NMDA-Glutamatrezeptor. Dies ist ein Merkmal, das es mit anderen Dissoziativa teilt. Hinsichtlich dieser Wirkungsweise ähnelt (erwartungsgemäß) Phencyclidin am ehesten Ketamin, seine Wirkung ist jedoch stärker psychotisch und weniger analgetisch. In Verbindung mit der Anwendung von Phencyclidin konnten insbesondere Benommenheit, Wahrnehmungsstörungen, Sprach- und Koordinationsstörungen, Störungen der Motorik (insbesondere Augenrollen, Gangstörungen), Speichelfluss, Paranoia, Halluzinationen und Aggressivität beobachtet werden. PCP ruft einen Rauschzustand hervor, welcher dem des akuten schizophrenen Schubs ähnlich sein soll. PCP löst dabei nicht nur die typische schizophrene Positiv-Symptomatik (z. B. Wahn, Halluzinationen, Ich-Störungen) aus, sondern auch die Negativ-Symptomatik (z. B. Apathie, Alogie, Affektverarmung, Anhedonie). Häufig sind ebenso Angstzustände in Form alptraumartiger psychotischer Episoden (bad trip). Phencyclidin kann, wie andere NMDA-Blocker auch, Hirnschädigungen verursachen. Phencyclidin ist toxischer und in seiner Toxizität komplexer als andere Dissoziativa. Die Schädigungen betreffen mehrere Hirnregionen und werden wahrscheinlich über verschiedene Rezeptorsysteme vermittelt.47 Nach häufigem Gebrauch von Phencyclidin wurden oft tagelang anhaltende Paranoia, Verwirrung, Aggressivität und unkontrollierte Halluzinationen auch ohne Einnahme der Droge beobachtet. Ob die Phencyclidinablagerung in Fettgewebe und Hirn (Depot-Wirkung) oder die Neurotoxizität dieser Substanz dies bedingt, ist nicht geklärt.
Aufgrund der eigentümlichen Pharmakokinetik nach oraler Applikation (im Magen liegt die Substanz in wasserlöslicher Form vor, die nur wenig resorbiert wird. Nach Übertritt in den Dünndarm wird durch die pH-Wert-Verschiebung eine höhere Fettlöslichkeit erreicht und die Substanz besser resorbiert. Mit der Verteilung im Blut kommt es zu einer Rückresorption in den Magen und damit zur erneuten Aufnahme über den Dünndarm.) ist die Wirkdauer nach oraler Zuführung erheblich verlängert, sodass das klinische Bild einer anhaltenden und fluktuierenden Intoxikation erklärt werden kann. PCP ist in den USA weiter verbreitet als in Europa. Entsprechende Schnelltests sind auf dem Markt. Nach einmaliger Einnahme ist PCP zwei bis fünf Tage im Urin nachzuweisen. Wegen der Ablagerung im Fettgewebe bei chronischem Gebrauch ist dann die Nachweisdauer wesentlich verlängert. In diesem Fall kann es zu tagelangen Rauschzuständen, Verwirrtheit und Wahnvorstellungen über Wochen bis hin zur Entwicklung einer Psychose kommen.
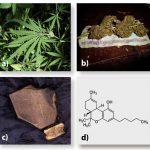
3.4.5 Cannabis (Abbildung 16a 16c)
Aus verschiedenen Hanfsorten der Gattung Cannabis können Rauschmittel gewonnen werden, die sich ebenfalls unter der Bezeichnung Cannabis zusammenfassen lassen. Die getrockneten und zerkleinerten harzhaltigen Blüten und kleinen Blätter der weiblichen Pflanze werden Marihuana genannt und unverändert konsumiert oder zu den Produkten Haschisch oder Haschischöl weiterverarbeitet. Cannabis ist in der Bundesrepublik Deutschland die am häufigsten konsumierte illegale Droge. Die Pflanze Cannabis indica bzw. Cannabis sativa wird seit ca. 9000 Jahren von den Menschen genutzt und gezüchtet. Sie stammt ursprünglich aus Zentralasien. Die Pflanze bildet in allen Teilen (außer in den Wurzeln und Samen) ein Harz, welches über 30 verschiedene Cannabinoide enthält; zu ihnen zählt auch Tetrahydrocannabinol. Im Allgemeinen hat indischer Hanf gegenüber dem Nutz-Hanf einen höheren relativen Anteil an beruhigendem Cannabidiol im Verhältnis zum Hauptwirkstoff. Ruderal-Hanf spielt für die Drogenproduktion kaum eine Rolle. Als Droge ist fast ausschließlich die weibliche, unbefruchtete Pflanze interessant, da diese die größte Wirkstoffkonzentration aufweist.
Die lange Geschichte des Gebrauchs als psychoaktive Droge und die juristischen (politischen) und medizinischen Probleme im Zusammenhang mit dem Gebrauch würden den Rahmen dieser Übersicht sprengen, es sei an dieser Stelle auf die entsprechende umfängliche Literatur verwiesen.10, 29, 43, 48
Die berauschende Wirkung der Hanfpflanze ist bedingt durch die darin enthaltenen Cannabinoide D9-Tetrahydrocannabinol (THC, Abbildung 16d) als aktiver Hauptmetabolit sowie Cannabidiol (CBD). Von 68 gefundenen Substanzen aus dem ätherischen Öl von Cannabis sativa wurden 57 identifiziert.48 Diese Substanzen binden an die Rezeptoren des Endocannabinoid-Systems im Zentralnervensystem des Organismus. Die endogenen Agonisten dieser Rezeptoren heißen Endocannabinoide und spielen eine wichtige Rolle bei der Modulation synaptischer Prozesse.29
Die bekanntesten Verwendungsformen sind:
· Marihuana: Die getrockneten, weiblichen Blütenstände, möglichst unbefruchtet (ohne Samen), mit oder ohne den anhängenden Blättern, werden geraucht (THC-Gehalt: 1 bis 12 %).
· Haschisch: Das gepresste Harz der Hanfpflanze wird geraucht oder, in Fett gelöst, zur Zubereitung THC-haltiger Getränke und Speisen verwendet.
· Haschischöl: Das mit Lösungsmitteln aus der Pflanze extrahierte Öl (das im chemischen Sinne allerdings kein Öl ist, sondern relativ reines THC) wird verdampft und eingeatmet, mit Tabak vermischt, auf Papier geträufelt und gelutscht, geraucht oder zur Zubereitung THC-haltiger Getränke und Speisen verwendet (THC-Gehalt bis zu 80 %).
· In der Medizin werden meist reines THC oder standardisierte Extrakte verwendet.
Je nach Anwendungsform variiert die Zeit bis zum Eintritt der Wirkung von einigen Minuten beim Inhalieren und zwischen 30 und 300 Minuten bei oraler Aufnahme. Die Wirkung hält selten länger als drei bis vier Stunden an, bei oralem Konsum werden aber auch deutlich längere Zeiträume berichtet. Cannabis kann unter anderem halluzinogen wirken, was sich meist in Form von leichten Wahrnehmungsveränderungen bei Farben, Formen, Geräuschen sowie der Zeitwahrnehmung äußert. Für die Wirkung von Cannabis und Haschischprodukten sind hauptsächlich folgende drei Hauptkomponenten verantwortlich, die sich in ihrer Wirkung wechselwirkend beeinflussen:
1. D9-Tetrahydrocannabinol (THC), welches zum Großteil den psychoaktiven Effekt von Cannabis hervorruft.
2. Cannabinol (CBN) ist vorrangig für die muskelrelaxierende (krampflösende) Wirkung verantwortlich.
3. Cannabidiol (CBD) wirkt dem THC-Effekt entgegen, schwächt damit dessen Wirkung und sorgt gleichzeitig für eine längere Wirkungsdauer des Gesamteffekts auf die körperlichen Prozesse. Ein hoher CBD-Anteil in den Trichomen schwächt den allgemeinen psychoaktiven Effekt und führt zu einer eher körperbetonten, sedierenden Wirkung anstatt zu einer bewusstseinserweiternden Erfahrung.48
Hanfpflanzen mit einer großen Anzahl von Trichomen (Pflanzenhaaren), mit sehr hohem THC- und einem extrem niedrigen Cannabidiolanteil-Verhältnis (in der Regel von der genetischen Varietät (Cannabis sativa oder Cannabis indica) und vom Reifegrad abhängig), führen demnach zum psychoaktiven Geisteszustand, den Konsumenten als klar, sauber und bewusstseinserweiternd empfinden. Konsumenten beschreiben den Rausch von Sativa-Gattungen meist als kopfbetont und geistesanregend, Indica-Gattungen hingegen werden eher als körperbetont und schmerzlindernd empfunden.
Ob und welche Gesundheitsfolgen durch Cannabiskonsum auftreten, ist umstritten und lässt sich pauschalierend nicht beantworten. Während Auswirkungen auf die Atmungsorgane und ein erhöhtes Krebsrisiko (beim Rauchen von Cannabis) weitgehend unbestritten sind, stellt sich die Datenlage bezüglich eventueller weiterer gesundheitlicher Auswirkungen auf die Psyche und die mögliche Entwicklung einer Abhängigkeit uneinheitlich dar. Es ist ungeklärt, ob und wenn ja, für welchen Personenkreis welche Dosis schädigend wirkt und ob unter Umständen bereits einmaliger oder seltener Konsum gesundheitliche Probleme bewirken kann. Es haben sich Anhaltspunkte ergeben, dass Cannabiskonsum bei bestimmten Personen das Risiko der Ausbildung einer Schizophrenie erhöht.
Die Deutsche Hauptstelle für Suchtgefahren e.V. ist der Auffassung, dass bei der speziellen Gruppe von Konsumenten, bei der Cannabiskonsum und zusätzlich persönliche und soziale Risikofaktoren zusammenkommen, eine besondere Gefährdung bestehe, welche folgendermaßen beschrieben wird:
Zwar hat der Konsument selbst ein Gefühl erhöhter Leistungsfähigkeit, die jedoch objektiv betrachtet immer mehr abnimmt. An die Stelle geordneten Denkens und logischer Schlussfolgerungen tritt häufig eine Art Scheintiefsinn, wovon vor allem Sorgfaltsleistungen betroffen sind. [ ] Im Zusammenhang mit dem genannten Amotivationssyndrom zeigt sich ein zunehmendes allgemeines Desinteresse, gepaart mit verminderter Belastbarkeit. Der Konsument zieht sich immer mehr in sich zurück und wird sich selbst und den Aufgaben des Alltags gegenüber immer gleichgültiger: Er fühlt sich den Anforderungen der Leistungsgesellschaft allmählich immer weniger verpflichtet, aber auch immer weniger gewachsen, und schert mehr und mehr aus seinem bisherigen sozialen Gefüge aus. (http://www.dhs.de/suchtstoffe-verhalten/illegale-drogen/cannabis.html, abgerufen am 13. Juni 2011)
Psychische Effekte treten bei folgenden Dosierungen auf: 3050 ?g/kg intravenös, 50 ?g/kg bei Rauchinhalation, 120 ?g/kg oral.49 Bei Rauchinhalation geringerer Mengen THC (57 mg) überwiegt die sedierende Wirkung, bei Mengen von 15 mg oder darüber überwiegt die bewusstseinsverändernde Wirkung, die sich bis zu psychotischen Zuständen steigern kann.30 Bei Rauchinhalation gehen ungefähr 20 % des im Rauch vorhandenen D9-THC in das Blut über, bei oraler Applikation nur etwa 6 %.50 THC geht vom Rauch sehr schnell ins Blut über, hierbei ist die Entwicklung der Plasmakonzentration mit intravenöser Einnahme vergleichbar. Bei oraler Einnahme in Form von Sesamölkapseln war die Wirkung wegen des First-Pass-Effekts vermindert, die Bioverfügbarkeit beträgt nur etwa 10 bis 20 %, die höchste THC-Konzentration wurde nach etwa zwei Stunden erreicht. THC ist im Blutplasma überwiegend an Proteine gebunden, maximal 10 % kommen in den roten Blutkörperchen vor. Die Plasmahalbwertszeit nach intravenöser Gabe entwickelt sich in vier Phasen, was nahelegt, dass es mindestens vier Gewebearten gibt, in die sich THC ablagert. Die THC-Konzentration fällt zunächst in wenigen Minuten stark ab, und sinkt dann langsam weiter. Die Halbwertszeiten betragen jeweils 1 Minute, 4 Minuten, 1 Stunde und 19 Stunden. Die kurzen Halbwertszeiten (1 und 4 Minuten, 1 Stunde) sind auf den schnellen Übergang von THC in bestimmte Gewebearten sowie auf den schnellen Stoffwechsel der Substanz zurückzuführen. Nach ungefähr sechs Stunden besteht ein Pseudogleichgewicht zwischen dem THC-Gehalt im Plasma und in den Geweben. Nach fünf Tagen werden etwa 80 bis 90 % der THC-Dosis in Form von Metaboliten ausgeschieden, etwa zu zwei Dritteln im Stuhl und zu einem Fünftel im Harn. Die THC-Konzentration im Gehirn erreicht nach rund 30 Minuten ihr Maximum, sie ist dabei etwa drei- bis sechsmal höher als im Plasma. Die THC-Konzentrationskurven im Gehirn und im Plasma verlaufen parallel, was für einen uneingeschränkten Übertritt ins ZNS spricht. Tierversuche haben gezeigt, dass sich THC als lipophile Substanz in bestimmten Gewebearten stark anreichert, zum Beispiel in Körperfett, Herz, Leber und Lunge. Ebenso wurde im Tierversuch nachgewiesen, dass THC durch die Plazenta auf Föten übergeht und deren Entwicklung beeinflusst, wobei die Auswirkungen noch nicht hinreichend erforscht sind.49,51
Cannabis wird in der Leber metabolisiert, die Metaboliten werden zum größten Teil biliär ausgeschieden. Mit Gaschromatografie / Massenspektrometrie lässt sich der einmalige Konsum bis zu 12 Tage nachweisen, da Cannabis sich im Fettgewebe anreichert. Bei regelmäßigem Gebrauch gelingt der Nachweis bis zu vier Wochen nach dem letzten Konsum.
Anders als bei Überschreitungen der definierten Alkoholgrenzwerte (etwa der 1,1 Promille-Grenze) wird die Fahrerlaubnis bei Fahrten unter Cannabiseinfluss nicht als unmittelbare strafrechtliche Folge entzogen. In Deutschland sorgten Urteile des Bundesverfassungsgerichts (Juni 2002, Dezember 2004) für eine gewisse Liberalisierung der bis dato relativ strengen Praxis der Behörden (siehe 2.6).
4 Schlussfolgerungen
Die Tatsache, dass eine Reihe von Drogen als illegal qualifiziert sind, führt häufig zu der Fehlannahme, der Konsum dieser Drogen sei gesetzlich generell verboten. Die gesetzliche Regelung bezieht sich jedoch ausschließlich auf den Besitz und die Verteilung der Drogen (nach §§ 29ff. des BtMG werden bestraft, wer Betäubungsmittel unerlaubt anbaut, mit ihnen Handel treibt, sie ohne Handel zu treiben, einführt, ausführt, veräußert, abgibt, sonst in den Verkehr bringt, erwirbt oder sich in sonstiger Weise verschafft). Daraus folgt für Betriebe und Einrichtungen die Notwendigkeit, den Umgang mit illegalen Drogen am Arbeitsplatz ebenso wie den mit anderen Suchtmitteln intern zu regeln, wenn sie den Konsum, oder besser den Nichtkonsum, nicht der alleinigen Verantwortung der Beschäftigten überlassen wollen.
Das Ziel der betrieblichen Suchtprävention, Punktnüchternheit am Arbeitsplatz, bezieht alle Arten von illegalen Drogen mit ein. Folgende Regeln können darüber hinaus für alle Beschäftigten unter Einbeziehung des Betriebs-/Personalrats verabschiedet werden (Hauptverband der gewerblichen Berufsgenossenschaften und Deutscher Verkehrssicherheitsrat 2007):
· Der Konsum illegaler Drogen unterbleibt während der Arbeitszeit und in den Pausen.
· Das Mitbringen illegaler Drogen an den Arbeitsplatz ist untersagt.
· Das Verteilen illegaler Drogen auf dem Gelände des Betriebes ist verboten und wird zur Anzeige gebracht.
· Ein Verstoß gegen eine der bevorstehenden Regelungen führt konsequent zur Intervention und zum Einstieg in den Stufenplan.
Den drogenfreien Betrieb oder die drogenfreie Verwaltung gibt es wahrscheinlich nicht. Betriebsärzte und Betriebsleitung müssen sich dieser Tatsache stellen. Sie müssen dabei auch realisieren, dass es nicht der Junkie ist, der ihnen am Arbeitsplatz begegnet, sondern ein Mitarbeiter, der ein relativ unauffälliges Erscheinungsbild zeigt. Bei den sogenannten Gelegenheitskonsumenten wird es in erster Linie um vereinzelte Tage mit Auffälligkeiten gehen. Solche Tage, an denen sich am Vortag in der Freizeit die Gelegenheit zum Drogenkonsum ergab. Da die konsumierten Wirkstoffe im Organismus teilweise langsam metabolisiert werden, kann es hier zu Auffälligkeiten kommen, wie es beim Restalkohol auch der Fall ist, wenn Beschäftigte akut nicht arbeits- bzw. dienstfähig sind. Die gesetzliche Grundlage für das Handeln in der akuten Situation wird für Unternehmen durch die Berufsgenossenschaftliche Vorschrift für Sicherheit und Gesundheit bei der Arbeit (BGV) und für den öffentlichen Dienst durch den jeweiligen Gemeinde-Unfallversicherungsverband (GUV) geregelt. Die Vorschriften sind in jüngster Zeit überarbeitet und um das Thema Einnahme von Medikamenten und Arbeitsfähigkeit ergänzt worden. Sie ersetzen den alten § 38 der Unfallverhütungsvorschrift.
Eine innerbetriebliche verbindliche Regelung zum Umgang mit Beschäftigten, die unter akuter Beeinträchtigung durch Substanzgebrauch stehen, ist in solchen Situationen hilfreich:
· Sie dient der Gleichbehandlung der Beschäftigten.
· Sie gibt Sicherheit für das konkrete Handeln der Betriebsleitung.
· Es entsteht Transparenz für alle Beschäftigten: Was passiert, wenn … ?
· Das Unternehmen nimmt den Arbeits- und Gesundheitsschutz ernst und erreicht damit ein gutes Image in der Öffentlichkeit.
· Vorgesetzte können das Handeln in der akuten Situation zum Anlass nehmen, mit Betroffenen bei deren Rückkehr an den Arbeitsplatz ein Klärungsgespräch über ihre Auffälligkeiten zu führen. Eine frühzeitige Intervention kann für beide Seiten von Nutzen sein.3
Diejenigen Mitarbeiter, die gewohnheitsmäßig Drogen konsumieren, werden das auf Dauer am Arbeitsplatz nicht kaschieren können. Hier wird es sich in der Regel vermutlich um eine psychische und/oder physische Abhängigkeit handeln. Dies kann aber nicht von der Betriebsleitung diagnostiziert werden, sondern hier ist der Betriebsarzt gefragt. Die Rolle der Betriebsärzte hat sich gewandelt. Sie sind laut Auftrag im Arbeits- und Gesundheitsschutz mehr Berater des Arbeitgebers und der Beschäftigten als ein Kontrolleur. Diese Rollenauffassung gilt auch für den Suchtbereich.2,23 Dementsprechend kann zusammenfassend empfohlen werden:
· Generelle Drogentests und Screenings im Betrieb entsprechen nicht den Prinzipien der Suchtprävention. In Risikobereichen sind sie durch Betriebsvereinbarungen zu regeln.
· Im Einzelfall, bei Auffälligkeiten am Arbeitsplatz in Verbindung mit Substanzgebrauch, kann den Beschäftigten ein Test zur Entlastung angeboten werden. Der Test erfolgt auf freiwilliger Basis mit Zustimmung der betroffenen Person.
· Als Unterstützung der Konsumreduzierung oder der Abstinenz können individuelle einzelvertraglich vereinbarte Konsumkontrollen geeignet sein
Literatur
1. Coper H. Psychopharmaka. In: Forth W, Henschler D, Rummel W (Hrsg.). Allgemeine und spezielle Pharmakologie. 5th edn BI Wissenschaftsverlag, Mannheim u.a., 1987:547568
2. Fleck J. Zwischen Tabuisierung und rigider Kontrolle rechtliche Aspekte des betrieblichen Umgangs mit Konsumenten illegaler Drogen in der Arbeitswelt. In: Illegale Drogen in der Arbeitswelt. Büro für Suchtprävention, Hamburg, 2000
3. Rimpl-Pegel U. Substanzbezogene Störungen am Arbeitsplatz. Herausgegeben von der Deutschen Hauptstelle gegen Suchtgefahren e.V., Hamm, 2008
4. Rascin C. Drug and alcohol testing in the workplace: moral, ethical and legal issue. Bull Narc 1993; 45: 4581
5. Bush DM. The U.S. mandatory guidelines for federal workplace drug testing programs: current status and future considerations. Forensic Sci Int 2008; 174: 111119
6. Lamberg ME, Kangasperko R, Partinen R et al. The finnish legislation on workplace drug testing. Forensic Sci Int 2008; 174: 9598
7. Magnavita N, Bergamaschi A, Chiarotti M et al. Workers with alcohol and drug addiction problems. Consensus document of the study group on hazardous workers. Med Lav 2008; 99(2): 358
8. Kauer JA, Malenka RC. Synaptic plasticity and addiction. Nat Rev Neurosci 2007; 8: 844858
9. Büttner A. Review: The neuropathology of drug abuse. Neuropathol Appl Neurobiol 2011; 37: 118134
10. Rätsch C. Enzyklopädie der psychoaktiven Pflanzen. 6th edn AT-Verlag Aarau 2002, 9940
11. Giannini AJ. An approach to drug abuse, intoxication and withdrawal. Am Fam Physician 2000; 61: 27632774
12. Die Drogenbeauftragte der Bundesregierung. Drogen- und Suchtbericht (Mai 2009). http://www.drogenbeauftragte.de
13. Geschwinde T. Rauschdrogen. 5th edn Springer-Verlag, Berlin u.a., 2003
14. Nutt D, King LA, Saulsbury W, Blakemore C. Development of a rational scale to assess the harm of drugs of potential misuse. Lancet 2007; 369(9566): 10471053
15. Nutt DJ, King LA, Phillips LD. Drug harms in the UK: a multicriteria decision analysis. Lancet 2010; 376(9752): 155865
16. Dolan K, Rouen D, Kimber J. An overview of the use of urine, hair, sweat and saliva to detect drug use. Drug Alcohol Rev 2004; 23: 213217
17. Verstraete AG. Detection times of drugs of abuse in blood, urine, and oral fluid. Ther Drug Monit 2004; 26: 200205
18. Drummer OH. Postmortem toxicology of drug abuse. Forensic Sci Int 2004; 142: 101113
19. Musshoff F, Junker HP, Lachenmeier DW, Kroener L, Madea B. Fully automated determination of amphetamines and synthetic designer drugs in hair samples using headspace solid-phase microextraction and gas chromatography mass spectrometry. J Chromatogr Sci 2002; 40: 359364
20. Musshoff F, Junker HP, Lachenmeier DW, Kroener L, Madea B. Fully automated determination of cannabinoids in hair samples using headspace solid-phase microextraction and gas chromatography mass spectrometry. J Anal Toxicol 2002; 26: 554560
21. Musshoff F, Lachenmeier DW, Kroener L, Madea B. Automated headspace solid-phase dynamic extraction for the determination of cannabinoides in hair samples. Forensic Sci Int 2003; 133: 3238
22. Musshoff F, Madea B. Review of biological matrices (urine, blood, hair) as indicators of recent or ongoing cannabis use. Ther Drug Monit 2006; 28: 155163
23. Hauptverband der gewerblichen Berufsgenossenschaften, Deutscher Verkehrssicherheitsrat (Hrsg.): Suchtprobleme im Betrieb. Alkohol, Medikamente, illegale Drogen. 5th edn Bonn, 2007
24. Jage J, Heid F. Anästhesie und Analgesie bei Suchtpatienten. Anaesthesist 2006; 55: 611628
25. Rundshagen I. Anästhesie und Analgesie bei Suchtpatienten. Anästh Intensivmed 2011; 52: 508519
26. Michelot D, Melendez-Howell LM. Amanita muscaria: chemistry, biology, toxicology, and ethnomycology. Mycol Res 2003; 107: 131146
27. Bauer W, Klapp E, Rosenbaum A. Der Fliegenpilz. AT-Verlag, Aarau, 2000
28. Boghdadi MS, Henning RJ. Cocaine: pathophysiology and clinical toxicology. Heart Lung 1997; 26: 46683
29. Julien RM. Drogen und Psychopharmaka. Spektrum Akademischer Verlag, Heidelberg u.a., 1997
30. Parnefjord R. Das Drogentaschenbuch. Georg-Thieme-Verlag, Stuttgart und New York, 2000
31. Freye E, Levy JV. Pharmacology and Abuse of Cocaine, Amphetamines, Ecstasy and Related Designer Drugs: A comprehensive review on their mode of action, treatment of abuse and intoxication. Springer-Verlag, Heidelberg u.a., 2009
32. Freye E. Opioide in der Medizin. 8th edn Springer, Heidelberg, 2009
33. Lehrmann E, Afanador ZR, Deep-Soboslay A et al. Postmortem diagnosis and toxicological validation of illicit substance use. Addict Biol 2008; 13: 105117
34. van Treeck B. Drogen- und Suchtlexikon. Lexikon-Imprint-Verlag, Berlin, 2003
35. Oyefeso A, Schifano F, Ghodse H et al. Fatal injuries while under the influence of psychoactive drugs: a cross-sectional exploratory study in England. BMC Public Health 2006; 6: 148160
36. Fereshteh SN, Kauer JA. LTP of GABAergic synapses in the ventral tegmental area and beyond. J Physiol. 2008; 15: 14871493
37. Hofmann A. LSD mein Sorgenkind. Die Entdeckung einer Wunderdroge. DTV, München, 2006
38. Nichols DE. Hallucinogens. Phamacol Ther 2004; 101: 131181
39. Wallach JV. Endogenous hallucinogens as ligands of the trace amine receptors: a possible role in sensory perception. Medical Hypotheses 2009; 72: 9194
40. Schultes RE, Hofmann A, Rätsch C. Pflanzen der Götter. AT-Verlag, Aarau, 1998
41. Lyttle T. Misuse and legend in the toad licking phenomenon. Int JAddict 1996; 28: 521538
42. Frohne D, PfänderHJ. Poisonous plants: A handbook for doctors, pharmacists, toxicologists, biologists and veterinarians. 2nd edn, Wiley-Blackwell, 2005
43. Ochse A. Naturdrogen und ihr Gebrauch. Nachtschatten Verlag, Solothurn, 2007
44. Zukin SR, Zukin RS. Phencyclidine. In: Lowinson JH, Ruiz P, Millman RB Langrod JG (Hrsg.). Substance Abuse. A Comprehensive Textbook. 2nd edn Wiliams & Wilkins, Baltimore 1992: 290302
45. Adams HA, Werner C. Vom Racemat zum Eutomer: (S)-Ketamin Renaissance einer Substanz? Anaesthesist 1997; 46: 10261042
46. Krystal JH, Karpeer LP, Seibyl JP et al. Subanesthetic effects of the noncompepetitive NMDA Antagonist, Ketamine, in humans: Psychotomimetic, perceptual, cognitive, and neuroendocrine responses. Arch Gen Psychiatr 1994; 51: 199214
47. Nakki R. Cerebellar toxicity of phencyclidine. J Neurosci 1995; 3: 20972108
48. Grotenhermen F (Hrsg.). Cannabis und Cannabinoide Pharmakologie, Toxikologie und therapeutisches Potenzial. Verlag Hans Huber, Bern, 2004
49. Huestis MA. Pharmacokinetics and metabolism of the plant cannabinoids, D9-tetrahydrocannabinol, cannabidiol and cannabinol. In: Handbook of Experimental Pharmacology 2005; 168: 657690
50. Aktories K, Förstermann U, Hofmann FB, Starke K. Allgemeine und spezielle Pharmakologie und Toxikologie. 9th edn Urban und Fischer, München, 2006
51. Fereshteh SN, Kauer JA. LTP of GABAergic synapses in the ventral tegmental area and beyond. J Physiol. 2008; 15: 14871493
52. Angelucci F, Ricci V, Spalletta G, Pomponi M, Tonioni F, Caltagirone C, Bria P. Reduced serum concentrations of nerve growth factor, but not brain-derived neurotrophic factor, in chronic cannabis abusers. Eur Neuropsychopharmacol. 2008; 18: 882887